La maladie de Chagas (trypanosomiase américaine)
Faits saillants
- La maladie de Chagas, causée par un parasite, le Trypanosoma cruzi, est transmise dans les déjections des triatomes, des insectes qui défèquent pendant qu’ils prélèvent du sang ou après l’avoir prélevé.
- La maladie est endémique en Amérique latine, mais en raison de la migration, on estime qu’il existe actuellement de six à sept millions de cas dans le monde, y compris 50 000 décès par année.
- La phase aiguë peut être asymptomatique ou inclure des signes et symptômes non spécifiques.
- Les enfants en phase aiguë sont plus susceptibles d’être symptomatiques que les adultes.
- La phase chronique se manifeste de dix à 30 ans plus tard et peut inclure des symptômes cardiaques ou gastro-intestinaux. Il n’est pas encore possible de prédire les 20 % à 40 % qui souffriront d’une atteinte cardiaque.
- La myocardiopathie de Chagas se détériore rapidement en insuffisance cardiaque et, souvent, en décès cardiaque subit.
- On estime que l’infection congénitale se produit chez 5 % à 10 % des nouveau-nés de mères infectées.
- On fait des tests de dépistage chez les donneurs de sang et dans le sang pour éviter la transmission de la maladie par le sang et les produits sanguins.
- Pendant la phase aiguë, on pose le diagnostic en décelant le parasite dans un frottis sanguin, tandis que pendant la phase chronique, on procède plutôt à une sérologie.
- En pédiatrie, le traitement au benznidazole ou au nifurtimox est recommandé dans tous les cas de maladie de Chagas congénitale, aiguë et chronique chez les enfants et les adolescents de moins de 18 ans et chez les femmes infectées en âge de procréer, afin d’éviter la transmission de la mère à l’enfant.
Introduction
Selon l’Organisation mondiale de la Santé, la maladie de Chagas est une maladie tropicale négligée et un indicateur de pauvreté et de défavorisation1. La maladie de Chagas (ou trypanosomiase américaine) un trouble multisystémique dégénératif chronique qui peut endommager les systèmes cardiovasculaire, digestif et nerveux central, est causée par le parasite Trypanosoma cruzi et est souvent transmise dans les déjections d’insectes infectés qu’on appelle les triatomes2. Ces insectes hématophages relativement gros (figure 1) vivent surtout en Amérique centrale, en Amérique latine et dans les régions du sud des États-Unis. Les insectes défèquent pendant qu’ils prélèvent du sang et après l’avoir prélevé. La personne mordue s’auto-inocule par inadvertance en frottant les déjections contenant le parasite dans une lésion de la morsure ou dans les membranes muqueuses de leurs yeux ou de leur bouche. La maladie peut aussi être contractée par la consommation d’aliments ou de boissons contaminés par les déjections des triatomes, par la transmission verticale d’une mère infectée à son bébé à naître ou (moins souvent) par une transfusion sanguine ou une transplantation d’organe2. La transmission verticale est observée dans une proportion estimative de 4 % à 7 % des nouveau-nés de mères infectées. La transmission orale est liée à un taux de mortalité plus élevé que la transmission vectorielle.
Figure 1 : Adulte femelle hématophage de l’espèce Triatoma rubida


Crédit photographique : Organisation mondiale de la Santé. Elmer Martinez/AFP – https://www.who.int/fr/news-room/fact-sheets/detail/chagas-disease-(american-trypanosomiasis)
L’épidémiologie
Selon l’OMS, de sept à huit millions de personnes de par le monde seraient atteintes d’une infection chronique par le T. cruzi4. Auparavant, la maladie de Chagas touchait surtout l’Amérique latine et l’Amérique centrale, mais en raison des migrations mondiales, on l’observe désormais également au Canada, aux États-Unis, en Europe, dans certains pays africains, ainsi que dans les régions de l’est de la Méditerranée et de l’ouest du Pacifique. Le réservoir primaire se situe en Amérique latine, où la maladie est endémique4. Les données sur la prévalence de la maladie de Chagas chez les nouveaux arrivants au Canada sont limitées, notamment chez les plus jeunes. D’après une étude, 3,5 % des immigrants au Canada en provenance d’Amérique latine étaient infectés par la maladie en 20064.
Les facteurs de risque
Les régions endémiques se situent au Mexique, en Amérique centrale et en Amérique du Sud 2,4. Tandis que des régions du sud des États-Unis présentent des cycles enzootiques de T. cruzi causés par les triatomes et les mammifères, notamment les ratons laveurs, les opossums et les chiens, la plupart des cas de maladie de Chagas sont diagnostiqués chez des immigrants en provenance d’autres pays 2,4.
La gravité de l’infection
L’infection initiale peut être asymptomatique. La maladie se décline en deux phases de gravités différentes2,4,5 :
- Première phase (aiguë) : Se manifeste peu après l’infection, par des symptômes non spécifiques bénins (voir le tableau 1) qui se résorbent au bout de deux à trois mois, sans traitement. Dans de rares cas, la maladie est grave et provoque une myocardite ou une méningoencéphalite qui peut être fatale. Les symptômes graves sont plus fréquents chez les enfants, les personnes âgées et les personnes immunodéficientes.
- Seconde phase (chronique) : La plupart des patients atteints d’une infection chronique à T. cruzi n’ont pas de symptômes. Cette phase chronique asymptomatique est dite de forme « indéterminée ». Cependant, dans 20 % à 30 % des cas, on observe une évolution grave de dix à 30 ans après l’infection initiale, Pendant la phase chronique symptomatique, des manifestations cardiaques peuvent se déclencher, y compris une myocardiopathie de Chagas accompagnée d’anomalies du système de conduction, un bloc de branche droit, un bloc cardiaque complet, des arythmies ventriculaires ou une insuffisance cardiaque congestive. Les manifestations gastro-intestinales incluent un mégaœsophage, un mégacôlon et une perte de poids6.
Les indices cliniques
La première phase (aiguë) et la seconde phase (chronique) de la maladie de Chagas s’associent à divers symptômes, résumés au tableau 15,6. En phase aiguë, de nombreux patients ne ressentent pas de symptômes ou seulement des symptômes légers.
|
Première phase : symptômes aigus |
Seconde phase : symptômes chroniques |
|---|---|
| Peuvent se manifester une ou plusieurs semaines après l’infection et persister de deux à trois mois | Peuvent se manifester de dix à 30 ans après l’infection initiale |
|
|
|
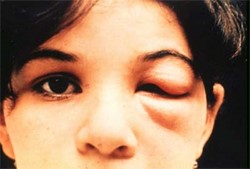
Source : Adapté du Gouvernement du Canada (voyage.gc.ca), Voyager à l’étranger, Santé voyage et sécurité, Maladies, Trypanosomiase américaine (maladie de Chagas) Figure 2. Le signe de Romaña est attribuable à la contamination des conjonctives par les déjections des triatomines
Crédit photographique : Centers for Disease Control and Prevention – https://www.cdc.gov/parasites/chagas/gen_info/detailed.html |
|
Le diagnostic
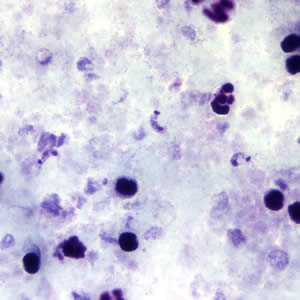
Le diagnostic de maladie de Chagas repose sur des tests de laboratoire après l’évaluation des observations cliniques et du risque d’infection du patient6. Le test dépend de la phase de la maladie. Pendant la phase aiguë, sur une période d’environ deux mois après l’infection initiale, les parasites peuvent être décelables dans des préparations fraîches de couches leucoplaquettaires ou de frottis sanguins (voir la figure 3) ou décelés par test PCR. On peut aussi les observer dans le liquide céphalorachidien. Après la phase aiguë, il faut effectuer au moins deux tests sérologiques pour déceler les anticorps du T. cruzi par la méthode d’immuno-absorption enzymatique (ELISA), par immunotransfert ou par anticorps immunofluorescents, auxquels il est possible d’accéder par l’entremise du Laboratoire national de microbiologie de Winnipeg.
Figure 3 : Trypomastigotes à T. cruzi dans un frottis sanguin
Goutte épaisse
Frottis mince
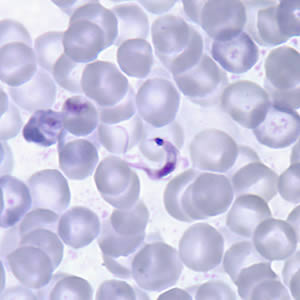
Source : Centers for Disease Control and Prevention. Bibliothèques d’images de la santé publique : https://www.cdc.gov/dpdx/trypanosomiasisamerican/index.html
Le dépistage
Les femmes enceintes à risque, leur nouveau-né et leurs enfants plus âgés
Les femmes enceintes à risque et tous les enfants d’une mère infectée par le T. cruzi devraient subir un test de dépistage de la maladie de Chagas7.
Figure 4 : Algorithme proposé par les hôpitaux universitaires de Genève, en Suisse, pour les femmes enceintes originaires d’Amérique latine
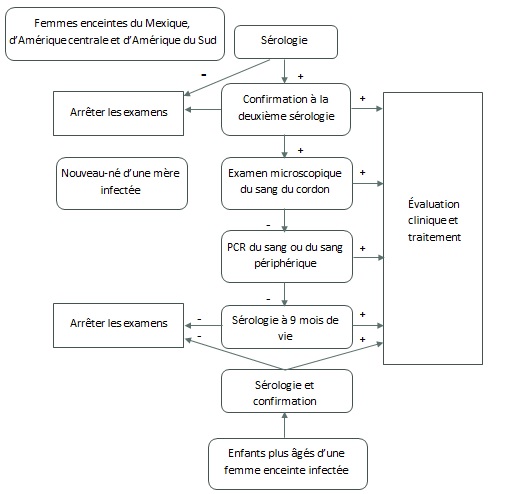
Traduction autorisée de Jackson Y, Myers C, Diana A et coll. Congenital transmission of Chagas disease in Latin American immigrants in Switzerland. Emerg Infect Dis 2009;15(4):601-3.
Les donneurs de sang et le sang
La Société canadienne du sang a ajouté des énoncés au questionnaire sur l’état de santé des donneurs, afin d’évaluer le risque que le donneur ait été exposé à la maladie de Chagas. Les donneurs se font demander s’ils sont nés au Mexique, en Amérique centrale ou en Amérique du Sud ou s’ils y ont passé au moins six mois continus et si leur mère ou leur grand-mère maternelle est née dans l’une de ces régions. Si les donneurs répondent « oui », ils sont soumis à un test de dépistage des anticorps contre la maladie de Chagas. Si le résultat est positif, les produits sont jetés, le donneur est avisé et l’information pertinente est transmise au donneur et à son médecin.
Le traitement
Il est recommandé de traiter la maladie de Chagas dans tous les cas de maladie congénitale, aiguë et chronique chez les enfants et les adolescents de moins de 18 ans 2,4. Les seuls antimicrobiens dont l’effet est démontré sont le benznidazole et le nifurtimox. Dans les deux cas, il faut faire une demande d’accès spécial à Santé Canada. Il est possible de vaincre la maladie si le traitement est amorcé peu après l’infection, mais l’efficacité du traitement diminue proportionnellement à la durée de l’infection. Un traitement peut également s’imposer pour soigner les symptômes. De nouvelles connaissances et de nouveaux outils sont disponibles, mais leur évolution dans le pipeline préclinique n’est pas approprié2,8. Même si la tératogénicité du benznidazole ou du nifurtimox n’est pas établie, par manque de données, le traitement n’est pas recommandé pendant la grossesse2.
La prévention
Il n’y a pas de vaccin contre la maladie de Chagas, mais des recherches sont en cours pour en créer un9. Le meilleur moyen de se protéger contre la maladie de Chagas pour les personnes qui voyagent ou résident dans des régions endémiques consiste à prévenir les piqûres de triatomes2 :
- Éviter de camper ou de dormir en plein air.
- Éviter la boue, les toits de feuilles de palmier ou les structures de briques d’adobe, qui sont vulnérables aux infestations.
- Utiliser des moustiquaires imprégnées d’insectifuge.
- Examiner les aires d’habitation pour déceler tout signe d’infestation et procéder à l’extermination, s’il y a lieu.
Pour en savoir plus sur la prévention des piqûres d’insectes, consultez le module intitulé Les maladies des voyageurs.
L’allaitement
Même si les données sont limitées, les mères atteintes de la maladie de Chagas peuvent continuer d’allaiter, à moins d’être en phase aiguë de la maladie, d’avoir réactivé leur maladie en raison d’une immunosuppression ou d’avoir des saignements aux mamelons10.
Quelques ressources
- Centers for Disease Control and Prevention. Parasites – American Trypanosomiasis (also known as Chagas Disease)
- Gouvernement du Canada. Trypanosomiase américaine (maladie de Chagas)
- Organisation mondiale de la Santé. Chagas (maladie de, trypanosomiase américaine)
Références
- Organisation mondiale de la Santé. Premier rapport de l’OMS sur les maladies tropicales négligées : Agir pour réduire l’impact mondial des maladies tropicales négligées. Genève : Organisation mondiale de la Santé 2011.
- Pérez-Molina JA, Molina I. Chagas Disease. Lancet 2018;391:82-94.
- Reisenman CE, Lawrence G, Guerenstein PG et coll. Infection of kissing bugs with Trypanosoma cruzi, Tucson, Arizona, USA. Emerg Infect Dis 2010;16(3):400-5.
- Lidani KCF, Andrade FA, Bavia L, Damasceno FS, Beltrame MH, Messias-Reason IJ, Sandri TL. Chagas Disease: From discovery to a world-wide problem. Front Public Health 2019;7:166.
- Norman FF, López-Vélez R. Chagas disease and breast-feeding. Emerg Infect Dis 2013;19(10):1561-6.
- Gouvernement du Canada. Maladie de Chagas (trypanosomiase américaine).
- Jackson Y, Myers C, Diana A et coll. Congenital transmission of Chagas disease in Latin American immigrants in Switzerland. Emerg Infect Dis 2009;15(4):601-3.
- Kratz JM. Drug discovery for Chagas Disease: A viewpoint. Acta Tropica 2019;198:105107.
- Rios LE, Vazquez-Chagoyan JC, Pacheco AO, Zago MP, Garg NJ. Immunity and vaccine development efforts against Trypanosoma cruzi. Acta Torpica 2019;200:105168.
- Norman FF, López-Vélez R. Chagas disease and breast-feeding. Emerg Infect Dis 2013;19(10):1561-6.
Réviseuse(s)
Noni MacDonald, MD